Anvisa anuncia novo plano de combate a irregularidades na importação e manipulação de canetas emagrecedoras
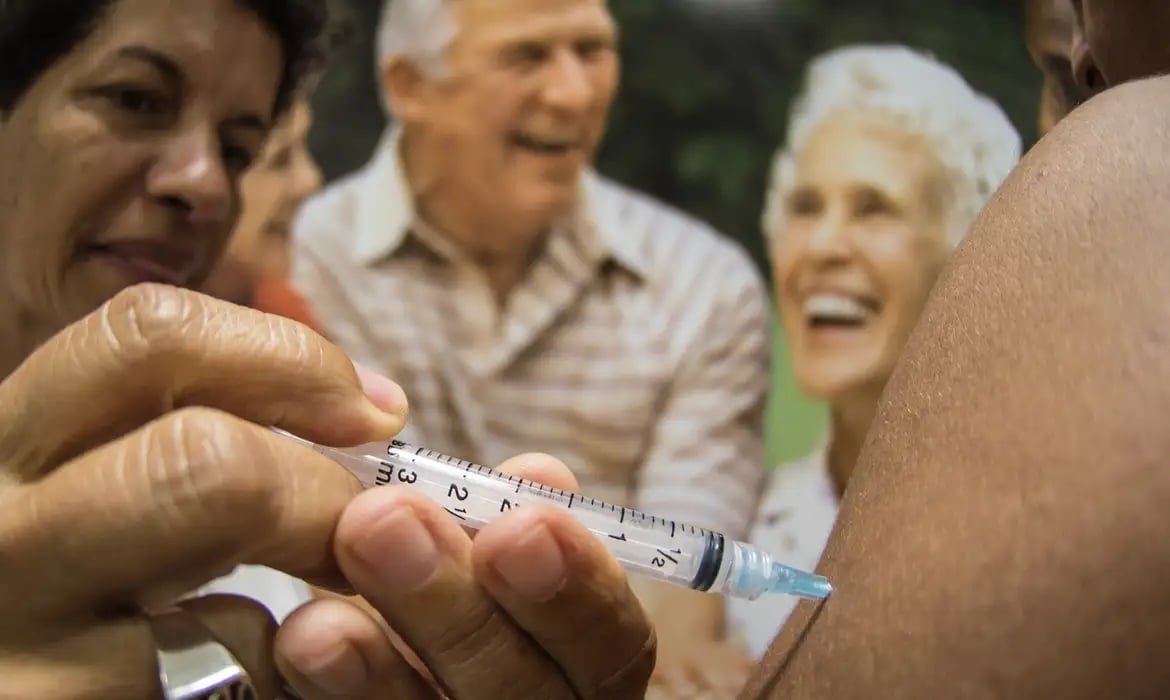
A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou, na última segunda-feira (6), um novo plano de ação estruturado que visa garantir a segurança de pacientes que utilizam medicamentos injetáveis de agonistas do GLP-1 — conhecidos como canetas emagrecedoras —, com princípios ativos de semaglutida, tirzepatida e liraglutida.
Dentre os seis eixos que compõem o plano de ação estão medidas previstas como a revisão das regras atuais do setor, a suspensão das autorizações de funcionamento para farmácias com situação de risco e novas fiscalizações em empresas importadoras de insumos para manipulação. Além disso, a Anvisa anunciou que vai intensificar as ações junto às Vigilâncias Sanitárias de estados e municípios e realizar acordos de cooperação com agências reguladoras de outros países.
Segundo a agência, as medidas ampliam a proteção e a segurança de medicamentos injetáveis de GLP-1 e foram motivadas pelo crescimento irregular da sua manipulação, que pode afetar a saúde dos pacientes. No segundo semestre de 2025, por exemplo, foram importados mais de 100 kg de insumos, os quais seriam suficientes para a preparação de, aproximadamente, 20 milhões de doses, número que, conforme alega a Anvisa, é incompatível com a realidade do mercado nacional.
Em 2026, a Anvisa realizou 11 inspeções em farmácias de manipulação e importadoras, as quais resultaram em oito interdições por problemas técnicos e falta de controle de qualidade. Entre os riscos mapeados pela agência estão a produção sem previsão de demanda por manipulação, problemas de esterilização, deficiências no controle de qualidade e a utilização de insumos farmacêuticos sem identificação de origem e composição.
Eixos do plano
O novo plano de ação da Anvisa inclui seis eixos estratégicos para ampliar a proteção e segurança de pacientes que utilizam essas medicações.
Eixo 1: Aprimoramento regulatório
- Revisão da nota técnica sobre procedimentos para importação, manipulação e controle sanitário de Insumos Farmacêuticos Ativos (IFAs) de agonistas de GLP-1;
- Revisão da resolução sobre boas práticas de manipulação de preparações magistrais e oficinais para uso humano em farmácias (RDC 67/2007).
Eixo 2: Monitoramento e fiscalização
- Intensificação de ações de fiscalização, especialmente de inspeções em importadoras, farmácias de manipulação e clínicas;
- Busca ativa de eventos adversos relacionados a medicamentos manipulados, com foco em serviços de emergência, hospitais e clínicas médicas;
- Aperfeiçoamento do controle sanitário sobre a importação de IFAs utilizados na produção e manipulação de agonistas do receptor GLP-1.
Eixo 3: Articulação institucional, federativa e internacional
- Criação de grupo de trabalho e celebração de acordo de cooperação com entidades médicas;
- Treinamento com o Sistema Nacional de Vigilância Sanitária (SNVS);
- Cooperação com agências reguladoras internacionais.
Eixo 4: Aprimoramento regulatório para análise de petições de registro de agonistas de GLP-1
- Priorização da análise dos cumprimentos de exigências das petições de registro;
- Harmonização do uso de guias técnicos de agências reguladoras de referência (ex: EMA e FDA).
Eixo 5: Comunicação com a sociedade
- Elaboração de plano de comunicação em linguagem simples;
- Orientação sobre riscos do uso indiscriminado;
- Informação sobre produtos irregulares;
- Esclarecimento sobre limites da manipulação magistral;
- Campanhas direcionadas a pacientes e profissionais.
Eixo 6: Governança
- Criação de grupo de trabalho na Anvisa para monitoramento e avaliação do Plano de Ação.
Com informações da Agência Nacional de Vigilância Sanitária.
Fonte: Brasil 61












Publicar comentário